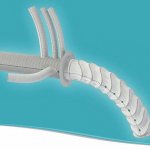
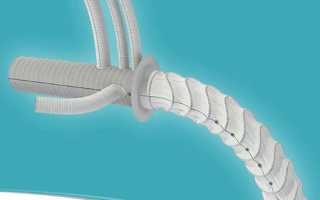
Впервые имплантация ксеноаортального клапана была проведена в Университете Британской Колумбии в 1981 г., а имплантация ксеноперикардиального в Университете Франсуа Рабле в 1984 г. Основные публикации относительно данных двух видов протезов были получены из этих двух центров. Клинические показатели были превосходными для протезов обоих типов, устанавливаемых в положении аортального клапана. Оба протеза содержат проволочный стент Elgiloy. Ксеноаортальный клапан является несоставным свиным клапаном, обработанным глутаральадегидом при давлении менее 2 мм рт.ст. Ксеноперикардиальный клапан имеет 3 отдельные, рассчитанные компьютером створки, обработанные глутаральдегидом с фиксацией при нулевом давлении. Если первый клапан является супрааннулярным биопротезом, не содержащим каких-либо интрааннулярных компонентов, то второй содержит супрааннулярное сшивающее кольцо и интрааннулярный компонент.
Биологические протезы, получившие распространение в хирургии пороков сердца еще в начале 70-х годов, по-прежнему востребованы в кардиохирургических клиниках благодаря улучшенным гидродинамическим характеристикам, низкой тромбогенностью и возможностью отмены приема антикоагулянтов. Биологические протезы широко используются в отделении неотложной кардиохирургии НИИ СП им. Н.В. Склифосовского при протезировании аортального клапана у пациентов старшей возрастной группы.
Цель: представить пятилетний опыт биопротезирования аортального клапана с использованием современных ксеноаортальных и ксеноперикардиальных протезов Carpentier-Edwards (Edwards Lifesciences, г. Ирвин, шт. Калифорния).
Материалы и методы исследования
В отделении кардиохирургии вспомогательного кровообращения и трансплантации сердца НИИ СП им. Н.В. Склифосовского за период с марта 2008 г. по июль 2010 г. были прооперированы 109 пациентов с пороком аортального клапана. Доминирующим диагнозом был аортальный стеноз у 84,4 % пациентов. Половой состав: мужчин – 51 (46,8 %), женщин – 58 (53,2 %). Средний возраст составил 66,5 ± 8,2 года. Большая часть пациентов относилась к старшей возрастной группе от 60 до 83 лет – 95 человек, 1 пациентка была в возрасте 28 лет, планирующая беременность в ближайшие сроки после операции, и 1 пациентка 32 лет, пожелавшая получить бесшумный протез. Большинство пациентов (94,5 %) имели правильный ритм сердца и относились к III–IV ФК по NYHA до операции.
рургическая коррекция порока аортального клапана выполнялась в условиях ИК с использованием фармакохолодовой кардиоплегии. Защиту миокарда осуществляли с введением раствора «Кустодиол» в коронарный синус. Температура охлаждения в среднем составила 32,1 °С (от 16,3 до 35,5 °С). Доступ к сердцу осуществлялся путем срединной стернотомии. После ссечения клапана проводилась очистка фиброзного кольца от остатков кальция и имплантация устройства в супрааннулярное положение с использованием П-образных швов 2-0 Ethibond (Ethicon, г. Брюссель, Бельгия). Наиболее частыми сопутствующими вмешательствами были: шунтирование коронарных артерий – 22 (20,2 %), протезирование митрального клапана – 20 (18,3 %), пластика или протезирование трикуспидального клапана – 25 (22,9 %), супракоронарное протезирование восходящей аорты (ВА) или пластика и экзопротезирование ВА – 18 (16,5 %), стентирование коронарных артерий – 14 (12,8 %). В ряде случаев операции проводили по программе «none-stop». В одном случае выполнили «расточку» фиброзного кольца. У 39 (35,8 %) пациентов были использованы ксеноаортальные биопротезы СЕ и у 70 (64,2 %) – ксеноперикардиальные протезы СЕ Perimount и Perimount Magna. Последнюю из указанных моделей использовали при малом корне аорты и необходимости имплантации протеза диаметром 19 мм – 9 (8,3 %) случаев. ительность искусственного кровообращения составила в среднем 130,9 ± 48,7 минут (от 51 до 327 минут), время интраоперационной ишемии миокарда 91,2 ± 33,2 минут (от 44 до 227 минут). В 69 (63,3 %) случаях к окончанию операции восстановление синусового ритма с достаточной ЧСС произошло без необходимости в использовании временного ЭКС. С целью определения гемодинамических характеристик работы клапана в послеоперационном периоде всем пациентам выполняли ЭХОКГ.
Результаты исследования и их обсуждение
Наиболее часто встречающимися в раннем послеоперационном периоде осложнениями были нарушения ритма, сердечная недостаточность, гидроторакс. Протез-зависимых осложнений в раннем послеоперационном периоде не отмечалось.
Госпитальная летальность составила 11 %. Из них в 5 (42 %) случаях была выполнена установка протезов размером 19 мм (СЕ Perimount-Magna) и в 7 (58 %) случаях – протезов бòльшего размера (СЕ, CE Perimount). Время искусственного кровообращения и пережатия аорты в этой группе превышало соответствующие средние значения в основной группе. В структуре причин летальности преобладала полиорганная недостаточность – 7 (58 %) случаев, немного реже отмечали сердечную недостаточность – 5 (41,7 %) случаев.
У всех пациентов перед выпиской не было отмечено регургитации на протезе по ЭхоКГ, среднее значение пикового систолического градиента давления на протезах диаметром 23, 21 и 19 мм составило 20,81 ± 6,2; 21,1 ± 9,7 и 26 ± 16,6 мм рт.ст. соответственно. Статистически достоверного различия в градиентах давления между ксеноаортальными и ксеноперикардиальными протезами не выявлено. Случаев дисфункции протезов в раннем послеоперационном периоде отмечено не было. Все пациенты первые 3–4 месяца получали антикоагулянты или дезагреганты с последующей отменой препаратов.
За пятилетний срок наблюдения за пациентами случаев биодеградации с кальцинацией, деформацией и нарушением функции протеза нами не выявлено.
Существуют определенные сомнения относительно гемодинамических показателей протезов сердечных клапанов малого размера – считается, что имеют место устойчивые послеоперационные градиенты и ограниченное снижение гипертрофии левого желудочка [1]. Во избежание потенциального риска несовместимости пациент-протез одной из целей протезирования аортального клапана должна являться имплантация протеза адекватного размера с определенными гемодинамическими характеристиками [2]. Большая часть применяемых в настоящее время механических и биологических протезов малого размера приводит, однако, к развитию значительных градиентов давления [3, 4, 5, 6]. Пациент, таким образом, обычно покидает больницу с остаточным послеоперационным аортальным стенозом, который может влиять на клиническое улучшение и долгосрочную выживаемость [7, 8].
Наиболее часто протезированию аортального клапана подвергаются пациенты пожилого возраста, имеющие аортальный стеноз и небольшой диаметр аорты.
ительный прием больными указанной возрастной группы антикоагулянтов зачастую противопоказан ввиду сложности контроля, что ограничивает применение у них механических протезов. В настоящее время биопротезы считаются наилучшим выбором для проведения операции протезирования аортального клапана у пациентов 60 лет и старше. Учитывая невысокую частоту возникновения структурных нарушений протеза в данной возрастной группе [9], изделия наверняка переживут своих реципиентов; другим преимуществом является возможность избежать антикоагуляции в данной популяции, характеризующейся повышенной риском осложнений. Каркасные биопротезы малого размера могут характеризоваться неудовлетворительными гемодинамическими параметрами, поскольку были отмечены высокие трансклапанные градиенты и субоптимальная площадь отверстия, что особенно актуально для протезов размером 19 мм [10]. Бескаркасные свиные клапаны могут обеспечить лучшую альтернативу [11], однако, как правило, они требуют более длительного времени ишемии при установке и их имплантация может быть сложнее, особенно при обызвествленном корне аорты, что нередко встречается у пожилых пациентов с пороком аортального клапана.
Анализ показал, что использование малых протезов размером 19 мм не являлось фактором, повышающим риск летальности. Однако следует учитывать необходимость проведения расширения отверстия у некоторых пациентов данной группы с целью имплантации клапана размером 19–21 мм.
о характеризует чрезвычайно малые диаметры отверстия у пациентов, что может привести к повышению риска ранней смерти во время операции. После вмешательств по Nicks et al. (15) или Manougian and Seybold-Epting (16) для имплантации протеза большего размера можно произвести расширение корня аорты. В то же время Sommers и David [12] установили что, по сравнению с изолированным протезированием аортального клапана у пациентов среднего возраста при расширении аортального отверстия лоскутом операционная летальность вдвое выше. Несмотря на то, что при расширении аортального отверстия показатели госпитальной летальности были выше, исследователи рекомендуют использовать данный метод для предотвращения несовместимости пациент-протез. Мы предполагаем, что за исключением чрезвычайно малых отверстий существенного преимущества в использовании метода расширения отверстия для пожилых пациентов, показатели внутрибольничной смертности для которых могут быть даже выше, чем приводимые Sommers и David [12], не существует. При этом также отсутствует значительное преимущество в показателях промежуточного выживания и выживания без клапан-ассоциированных осложнений. Наш опыт использования ксеноаортальных биопротеов Carpentier-Edwards и наши предварительные результаты на ограниченном числе пациентов показали, что указанные протезы обеспечивают клиническое улучшение и значительное снижение все еще остающейся выше границ нормы массы левого желудочка. Настоящее исследование имеет определенные ограничения, преимущественно обусловленные малым числом пациентов и коротким сроком последующих эхокардиографических наблюдений. Однако удовлетворительные результаты, полученные на ранних стадиях и показывающие хорошие гемодинамические показатели, вдохновляют нас поверить в возможность дальнейших улучшений показателей при долгосрочном наблюдении у пациентов с имплантированным биопротезом Carpentier-Edwards Perimount.
В предыдущих работах указывалось, что биопротезы Carpentier- Edwards Perimount характеризуются долгим сроком службы и отсутствием структурного разрушения [13,14]. Такие наблюдения вкупе с результатами настоящего исследования подтверждают возможность использования биопротезов в качестве подходящего варианта при выборе протеза аортального клапана для пациентов пожилого возраста с малым диаметром аортального отверстия.
Выводы
1. Наиболее значимыми факторами риска госпитальной летальности при протезировании аортального клапана современными биологическими протезами являются выраженная сердечная недостаточность и полиорганная недостаточность.
2. Современные ксеноаортальные и ксеноперикардиальные биопротезы Carpentier Edwards в аортальной позиции обеспечивают хорошую транпротезную гемодинамику и отсутствие протезозависимых осложнений на раннем послеоперационном этапе.
3. В настоящее время протезирование аортального клапана биологическими протезами по нашим наблюдениям является «операцией выбора».
Показания к проведению операции
Показанием для удаления аневризмы является уже факт ее наличия, в том числе, если даже симптомы заболевания не проявляются. Метод и сроки лечения определяются с учетом размеров аневризмы, ее локализации, вероятности разрыва, состояния организма и возраста пациента. В Москве множество клиник предоставляют услуги по обследованию, диагностике и лечению заболеваний сосудов, в том числе и аневризмы аорты.
Операция обязательна при:
- наличии разрыва и последующего кровотечения (экстренное оперативное вмешательство);
- прогрессирующем увеличении объемов выпячивания – в год больше 4 мм;
- аневризме больше, чем 5 см в диаметре;
- вероятности появления разрыва, эмболии или тромбоза;
- нарушенной циркуляции крови в нижних конечностях;
- диагностированном расслоении стенки аорты в области аневризмы (у пациента при этом возникает сильная боль в области грудной клетки, паху, животе).
Дополнительные факты
Если клапанный аппарат относительно сохранен (нет грубых фиброзных изменений, кальцификации клапанов и т. Д. ), То предпочтение отдается пластике митрального клапана. Если невозможно восстановить митральный клапан с использованием аутотканей, выполняется его протезирование. При замене митрального клапана используются искусственные (механические) и тканевые (биологические) протезы.
Механические протезы (откидные, шариковые, дисковые) оснащены фиксирующими элементами разных типов, изготовленными из искусственных материалов — силикона, графитовых смесей и заключенными в металлическую раму. После протезирования митрального клапана с помощью искусственного протеза необходимо антикоагулянтное лечение в течение жизни и контроль коагулограммы из-за риска тромбоэмболических осложнений.
У пациентов с высокой известной вероятностью тромбоза (мерцательная аритмия, увеличение размеров полостей сердца, тромбоз левого предсердия, тромбофлебит) и невозможностью проводить антикоагулянтную терапию (при метроррагии, язвенной болезни, мочекаменной болезни и ), Как и у пожилых людей, протезирование митрального клапана является предпочтительным.
Протезы ткани снабжены запирающий элементом естественного биологического происхождения (xenoklapany перикарда и аортальный, allocaplanes всей жесткой твердой-клапан сохранилась в растворе глутаральдегида), закрепленную на опорной раме металла или полимера. Преимуществами биопротезов являются лучшие гемодинамические свойства, меньший вес и размер, меньший тромбогенный эффект по сравнению с искусственными протезами.
Ограничением использования тканевых протезов в протезах митрального клапана является их биодеградация в отдаленные периоды (кальцификация, разрыв клапана). Перед планированием операции по замене митрального клапана определяются сократительная функция миокарда, дисфункция клапана и его тяжесть. Типичная схема обследования, которую кардиолог назначает перед заменой митрального клапана, включает эхокардиографию, рентгенографию, фонокардиографию, ЭКГ.
Начиная со второго дня после операции, пациентам назначают антикоагулянты (гепарин). Разовая доза определяется индивидуально с учетом динамики тромбоэластограммы, чтобы получить умеренную гипокоагуляцию, которая предотвращает тромбоз. На пятый день после протезирования митрального клапана начинается снижение дозы гепарина и вводятся непрямые антикоагулянты. Отмена гепарина проводится с нормализацией показателей PTI (40-60%) или МНО (2,0-3,0 — для тканевых протезов, 2,5-3,5 — для искусственных протезов). В будущем пациенты, перенесшие протез митрального клапана с механическим протезом, остаются в постоянном потреблении непрямых антикоагулянтов с регулярным мониторингом INR (PTH). Пациенты с имплантированными биопротезами получают антикоагулянты в течение шести месяцев после протезирования митрального клапана. Таким образом, при нормальном функционировании биопротеза антикоагулянты отменяются. При появлении признаков гипокоагуляции (кровотечение из носа, десен, гематурия) уменьшите дозу препарата под контролем МНО (ПТГ). В случае развития неконтролируемой гипокоагуляции, появления симптомов внутриполостного кровотечения пациент срочно госпитализируется. В первой половине года после протезирования митрального клапана пациентам назначают ограничение нагрузки, рациональный водно-солевой режим, диету с высоким содержанием магния и калия. Обычная консультация кардиохирурга проводится через шесть месяцев после протезирования митрального клапана.
Основные аспекты протезирования аорты
При этой патологии главным принципом оперативного вмешательства является замещение искусственным протезом патологического участка аорты. При открытом типе операции это достигается удалением подобного участка и сшиванием аорты с установленным протезом по методу «конец в конец», при внутрисосудистых малоинвазивных операциях – помещением искусственного шунта внутрь аорты, не удаляя при этом аневризму.
Реже производят резекцию мешотчатой аневризмы, при этом стенки аорты ушиваются, шунт не устанавливается; и паллиативные операции (к примеру, операции при которых для предотвращения дальнейшего расширения аорты, ее окутывают тканью из синтетического материала).
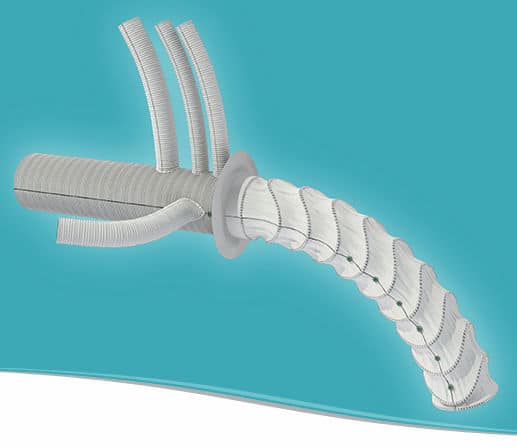
Виды имплантатов
Имплантаты между собой имеют некоторые отличия. Они бывают механическими и биологическими.
Механические
Их достоинствами являются:
- Стандартность производства.
- Сохранение прочности длительное время.
Недостатки это:
- Необходимость регулярного приема препаратов из группы антикоагулянтов.
- Ряд моделей недолговечны.
- Неестественная форма.
Биологические
Их достоинства это:
- Центральный кровоток осуществляется через клапан.
- Небольшая необходимость приема препаратов из группы антикоагулянтов.
Их недостатками являются:
- Возможность дегенерации материала.
- Неизвестен точный срок эксплуатации.
- Относительно большой трансклапанный градиент давления.
Перед проведением операции делают компьютерную томографию
Подготовка к процедуре
При разрыве аневризмы, на подготовку времени критически недостаточно, ввиду этого больному срочно производят анализы крови и мочи, проверяют показатели свертываемости крови (коагулограмма), УЗИ, КТ, после этого делают операцию.
Если на аорте производится плановая операция, то осуществляют более тщательное обследование больного. Делают рентгенографию грудной клетки, ЭКГ, УЗИ органов брюшной полости, магнитно-резонансную и компьютерную томографию, которые помогают точно определить локализацию аневризмы, ее строение и размеры, делают анализы крови и мочи.
На этапе подготовки к операции больной должен оповестить доктора о принимаемых им лекарствах. В особенности если он принимает аспирин или другие антикоагулянты, способные привести к снижению свертываемости крови и последующему возникновению кровотечения.
При поступлении пациента в условия стационара у него уже есть большая часть результатов исследований, некоторые, иногда, еще раз проводятся в клинике.
Перед операцией, вечером, есть можно не позднее 8 ч до хирургического вмешательства, также больной принимает душ, одевает чистую одежду и после этого ложится спать. При наличии переживаний и невозможности уснуть разрешается принять снотворные и седативные препараты.
При проведении открытых операций, производимых на аорте необходим общий наркоз, иногда – подключение больного к системе искусственного кровообращения либо установка временного шунта. При эндоваскулярном типе лечения может быть использована местная анестезия. Продолжительность открытой операции составляет примерно от 3 до 6 ч.
Стоимость оперативного лечения
В большинстве случаев операция по замене аортального клапана проводится бесплатно. Это обусловлено наличием квот, которые предоставляет здравоохранение РФ по системе ОМС. Но если воспользоваться такой квотой нет возможности, или по каким-либо причинам пациент получил отказ, у него имеется вариант проведения операции за свой счет. Хирургические вмешательства такого рода считаются вполне доступными для рядовых граждан и проводятся во всех крупных городах России.
Стоимость оперативного лечения варьируется в диапазоне 90-200 тысяч рублей. В Москве этот показатель немного отличается и составляет 65-600 тыс. Причем увеличение цены напрямую зависит от объема и сложности манипуляций.
Стандарты протезирования клапана сердца за границей на порядок выше, поэтому зачастую пациенты выбирают зарубежные клиники. В различных странах стоимость операции по замене имеет существенные отличия.
| Страна | Стоимость/евро |
| США | 120000 |
| Израиль | 50000 |
| Сингапур | 30000 |
| Испания | 24000 |
| Польша | 20000 |
| Турция | 10000 |
| Мексика | 9000 |
| Индия | 4000 |
Учитывая многочисленные отзывы пациентов, можно сделать вывод, что лечение как за рубежом, так и в РФ отличается высоким качеством и проводится на достойном уровне.
Хирургическая тактика и техника операции
Операции по протезированию аорты для каждого вида аневризмы имеют ряд отличий.
Операция по лечению аневризмы брюшной аорты
На аорте чаще аневризма локализуется в области брюшной полости.
Даже недолгое перекрывание сосуда может привести к острой недостаточности почек, ввиду этого хирургическое вмешательство производится за максимально короткое время.
Вскрыв брюшную полость, кишечные петли сдвигаются врачом вправо, он выделяет подвздошные и почечные сосуды, мочеточники, определяет границы аневризмы, пережимает все сосуды, которые входят в область выпячивания.
При наличии аневризмы в брюшной аорте главным видом операции является протезирование. Протез при этом бывает изготовлен в форме трубки, которая после иссечения соединяет концы аорты выше и ниже выпячивания.
При дополнительном наличии атеросклероза в тяжелой степени в месте, где аорта разветвляется на подвздошные артерии, применяют бифуркационный протез (имеющий форму наподобие развилки). Он фиксируется к 2 подвздошным артериям и аорте. Само выпячивание и место, где производилась бифуркация аорты, подвергаются удалению.
Бифуркационный протез аорты
При наложенных зажимах с верхней и нижней сторон аневризмы, в полость сосудов с обеих сторон пережатого места, чтобы предотвратить образование тромбов вводится гепарин. После этого производят рассечение стенки аневризмы, удаление из нее тромботических масс, осуществляют промывку полости сосуда гепарином и производят иссечение передней и боковых стенок.
Верхняя сторона протеза пришивается к верхней стороне аорты, при этом швы накладываются кнаружи. Потом, к аорте, бедренным либо подвздошным артериям фиксируют нижний конец протеза.
После того, как протез установлен, снимают зажимы с аорты, и кровоток по ней восстанавливается. Хирургическое вмешательство осуществляется с применением временно установленного анастомоза, направляющего кровь в обход места операции, либо используют систему искусственного кровообращения.
При окончании операции специалист удостоверяется в отсутствии кровотечения и надежно ли зафиксирован швами протез, осуществляет укладку кишечника в нужное положение и затем производит ушивание тканей. Чтобы предотвратить возникновение свищей из-за влияния на кишечные петли нитей швов, на протез накладывается 2 слоя брюшины.
После операции в течение некоторого времени возникают дисфункции кишечника – вздутие, по этой причине для предотвращения расхождения на брюшной стенке шва, его укрепляют нитью из нейлона либо проволокой.
Техника лечения аневризмы в грудном и восходящем отделах
При наличии выпячивания в восходящей аорте и ее дуге, патологический участок также протезируют.
При аневризме начальных отделов аорты делают операцию открытого типа. Для этого специалист делает продольное рассечение грудной клетки, вскрывает перикард, потом производится подключение больного к системе искусственного кровообращения. Циркулирующая во время хирургического вмешательства через аппарат кровь, охлаждается, а для обеспечения ею венечных сосудов в них вводятся катетеры.
После выделения аневризмы, на ее края ставят зажимы, иссекают стенку, удаляют патологические части и фиксируют протез. Чаще в его качестве применяются сосуды самого пациента либо другие его ткани.
При наличии кроме аневризмы, патологии в аортальном клапане, при операции может быть выполнена его пластика. После завершения операции, специалист проверяет надежность фиксации протеза, пациента согревают до оптимальной температуры, и когда левый желудочек сердца заполнится кровью до достаточного количества для его нормальной сократительной функции, отключают аппарат искусственного кровообращения.
При окончании операции в правую плевральную полость и сердечную сумку осуществляют установку дренажей, ушивают каждый слой тканей, грудную клетку фиксируют проволокой либо скобами из металла.
При протезировании восходящей аорты, если шейка аневризмы узкая, кровообращение больного сохраняют в нормальном режиме. В области основания аневризмы аорты ставят зажим, аневризму целиком удаляют, место ее отхождения надежно ушивают.
При локализации выпячивания в дуге аорты доступ осуществляется через полость левой стороны грудины, грудная клетка в косом направлении иссекается и затем разрез направляется в правую сторону, в промежуток между 2 и 3 ребрами. Оперативное вмешательство осуществляется с сопутствующим использованием системы искусственного кровотока, а для кровоснабжения головы, между сонными артериями и нисходящей частью сосуда производят установку шунта.
После того, как шунт установлен, пережимают аневризму и затем удаляют, в этом месте вставляется и фиксируется протез, и к нему специалист подшивает те сосуды, которые в норме отходят от дуги аорты. После того, как оптимальные показатели кровотока восстановлены, удаляют шунт, и пациента отключают от системы искусственного кровообращения.
После всех этих манипуляций, специалист производит полное удаление выпячивания аорты. Целостность сосуда можно восстановить, использовав прямой протез, который соединяет концы грудного отдела аорты. Иногда в месте, где удалена аневризма, аорту зашивают целиком, а кровообращение обеспечивает временный анастомоз, становящийся впоследствии постоянным.
Эндопротезирование стент-графтом
При плановом лечении заболевания производятся малоинвазивные операции. Эндоваскулярное вмешательство представляет собой введение катетера через бедренную артерию. Он доставляет к участку сосуда с наличием патологии стент-графт, который обеспечивает «выключение» аневризмы из кровообращения.
Этот прибор является пружиной из металла, которая расправляется в полости аорты до необходимого диаметра. Снаружи на стенте установлена прочная основа из синтетической ткани. Стенты бывают прямого типа и бифуркационные, устанавливаемые в месте разветвления сосуда.
Стент-графт создают вручную, для каждого больного индивидуально, с использованием материалов высокого качества, поэтому изделие дорогое и для широкого круга пациентов малодоступно.
Жизнь с новыми клапанами
Длительность возвращения к обычной жизни зависит от точного выполнения рекомендаций врача. Это же определяет и долговечность работы протеза, отсутствие осложнений после операции.
Ограничения
Запрет на курение после протезирования клапана Не нужно полностью отказываться от физической активности, но она должна быть строго дозированной.
Вождение автомобиля и занятия спортом могут быть только после согласования с врачом. Длительные поездки нежелательны, особенно первые месяцы. Поэтому нужно как можно чаще останавливаться для того, чтобы немного пройтись.
Большой вред приносит курение сосудам, так как это один из факторов их сужения и закупорки атеросклеротическими бляшками. Кроме этого, никотин и смолы нарушают очистку легких, повышают нагрузку на сердце. Поэтому курение, как и алкоголь, ослабляющий миокард, должны быть исключены для успешного результата лечения.
Лекарственная терапия
Если был использован в качестве протеза биологический аналог, то назначают препараты, тормозящие иммунный ответ организма для профилактики отторжения.
При признаках гипертонии или стенокардии их терапия продолжается в соответствии с советами кардиолога. Если состояние не стабилизируется, то обязательно повторно нужно обратиться к врачу для коррекции дозы.
Антикоагулянтная терапия обязательно проводится под контролем свертывающей активности крови.
Возможность работать
Большинство пациентов восстанавливает трудоспособность в полном объеме. Некоторым нужно перейти на легкий труд, может быть определена и группа инвалидности. Это определяется состоянием пациента, сопутствующими заболеваниями, причиной операции и характером труда на рабочем месте.
Физические нагрузки
Не нужно полностью отказываться от физической активности, но она должна быть строго дозированной. Оптимальным вариантом в первое время будут пешие прогулки, лечебная физкультура и дыхательные упражнения.
Диета
Ограничения в рационе касаются животных жиров, сахара и мучных изделий, поваренной соли, острых приправ и кофе. Полезны нежирные сорта рыбы и мяса, ягоды, фрукты, салаты из свежих овощей с растительным маслом, сухофрукты, отруби.
Если установлен биопротез, то уменьшают содержание кальция в питании. Он содержится в молочных продуктах, орехах, бобовых и семенах.
Противопоказания
Для планового лечения выпячивания аорты есть ряд противопоказаний – острая форма сердечного инфаркта, инсульт, тяжелые дисфункции почек и печени, наличие тяжелой сердечной недостаточности. У пациентов в возрасте более 75 лет, при наличии низкого уровня гемоглобина и повышенном содержании креатинина, операция может иметь неблагоприятный исход, в особенности при разрыве. Если возник разрыв аневризмы, то противопоказаний к операции нет, потому что без хирургического вмешательства происходит летальный исход.
Есть два вида операции при аневризме – это паллиативные и радикальные. Паллиативные используются только при наличии противопоказаний к открытой операции, и при высокой вероятности разрыва выпячивания. Радикальные делают намного чаще, они являются главным видом лечения нарушения.
Оценка результатов аортального протезирования
Выживаемость больных равна примерно 81-95% в первый год после хирургического лечения, на протяжении 5 лет – 73%-92%, 10 лет – 60%-73%, 14 лет – 48%-67% . Причины отдаленной смертности – это патологический процесс в брахиоцефальных артериях, аортальная недостаточность, высокий класс NYHA.
Может возникнуть необходимость в повторных оперативных вмешательствах из-за нарушения функции ауто- либо аллографтов, биопротезов. Отсутствие необходимости в повторных операциях на протяжении 5 лет равна 93-97%, 89%-95% – 10 лет, и 82-87% – 15 лет.
После операции необходимо периодически осуществлять замер показателей артериального давления
Причины для замены клапанов
Чаще всего протезирование проходит на клапанах левой половины сердца – митральном и аортальном, так как они подвержены нагрузке высоким артериальным давлением, ревматическому поражению. Операция проводится только в том случае, если все остальные методы не принесли результата.
Аортального
Замена клапана аорты бывает при стенозе или недостаточности, как изолированных, так и сочетающихся одновременно между собой или с другими пороками сердца. Показаниями является кальциноз, рубцовая деформация, нарушения внутрисердечной и системной гемодинамики.
Митрального
При грубых изменениях створок, пролапсе с недостаточностью кровообращения митральный клапан нужно заменить искусственным. Если диагностирован септический эндокардит, то дополнительными факторами необходимости установки протеза могут быть:
- отсутствие результата от интенсивной терапии антибиотиками,
- нарастание декомпенсации кровотока,
- высокий риск тромбоэмболии,
- УЗИ выявило разрастание эндотелия и разрушение створок.
Рекомендуем прочитать статью о комбинированном пороке сердца. Из нее вы узнаете о видах пороков сердца и их симптомах, проведении диагностики и методах лечения, возможных осложнениях и прогнозе для больных.
Легочной артерии
Неплотное смыкание при тетраде Фалло, синдроме Марфана, легочной гипертензии может вызывать необходимость замены клапана.
Стеноз устья пульмональной артерии редко требует протезирования, так как устраняется при помощи рассечения сросшихся створок.
Трикуспидальный
Основная причина поражения трехстворчатого клапана – ревматизм. Он может протекать в виде воспаления самих створок, внутренней оболочки или всех слоев сердца. После ликвидации острых проявлений части клапана срастаются, становятся жесткими и деформированными, заменяются рубцовой тканью. При выраженной правожелудочковой недостаточности проводится хирургическое лечение с установкой искусственного протеза.